
第10回「女性の病気(治療編)」
乳がん、子宮がん、卵巣がん、不妊症
昨年3月号にリニューアルした新「医療最前線」では、早期発見を目的に、診断をメインに紹介してきた。今月号からは、その「治療編」として各診療科の専門的な治療内容をわかりやすく紹介する。
第10回は「女性の病気」について各分野の専門医が解説する。
【乳がん】「ホルモン受容体」&「HER2」の4タイプに応じた治療

乳腺・内分泌外科
島 宏彰講師
乳がんは、①ホルモン受容体が関わって発症するがんと②増殖因子の「HER2(ハーツー)」が関わって発症するがんがあり、それぞれ「陽性」と「陰性」があって全部で4タイプ(サブタイプ)がある。
乳がんの治療は、このサブタイプによって異なる(表)。
「HER2」が陽性の場合には①「抗HER2療法」を中心とした治療を行う。ホルモン受容体が陽性で「HER2」が陰性のタイプは、主に②「内分泌療法」が基本となる。
「HER2」「ホルモン受容体」ともに陰性(この場合、多くはふたつの受容体ともに陰性であり、トリプルネガティブと言われることもある)の場合には、主として③「抗がん剤治療」が行われる。③の場合には、最近では免疫チェックポイント阻害剤が使われるようになっており、適用されることもある。
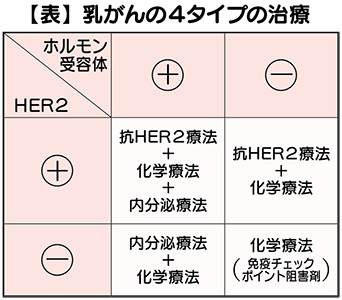
このように乳がんの治療にはサブタイプによる4つのタイプが重要で、タイプごとに治療薬が決まっていて、それぞれに応じた治療を選択することになる。
そこでそれぞれの治療について説明する。
まずは①「抗HER2療法」。「HER2」が陽性の場合には、細胞膜に「HER2」という細胞の増殖を非常に進めてしまう物質が発現していて、それが細胞増殖を促すシグナルを出す。それを阻害するのが①「抗HER2療法」である。薬剤の「ラスツズマブ」が有効で、「ラスツズマブ」が「HER2」に特異的に付着し「HER2」が細胞増殖を促すシグナルを止める。また「ラスツズマブ」に「ベルツズマブ」を併用することもある。
②「内分泌療法」は、がんの栄養となる「エストロゲン」の取り込みを抑制する「タモキシフェン」や「アロマターゼ阻害剤」が用いられる。
「エストロゲンが存在するとそれを栄養とするがん細胞が増えてしまうので、エストロゲンの取り込みをブロックすることで細胞周期をブロックし、さらに状況により細胞周期の制御に関わるサイクロン依存性キナーゼ(CDK)を阻害する『CDK4/6阻害剤」を併用する場合もあります」と札幌医科大学の島宏彰講師。
③「抗がん剤治療」で使われる「免疫チェックポイント阻害剤」は、がん細胞が免疫細胞(T細胞)にかける「攻撃停止ブレーキ」を解除し、からだ本来の免疫でがんを攻撃させる治療薬だ。がん細胞が持つ、免疫細胞にブレーキをかける信号を遮断することで、再活性化したT細胞ががんを攻撃する。
がん細胞は、表面に「PD─L1」というタンパク質を発現させ、T細胞の「PD─1」という受容体と結合することで「攻撃を停止せよ」という信号(ブレーキ)を送るが、免疫チェックポイント阻害剤は、T細胞の「PD─1」またはがん細胞の「PD─L1」に結合し、このブレーキ信号をブロックする。ブレーキが解除されたT細胞は、再びがん細胞を認識し、攻撃を開始して死滅させる。
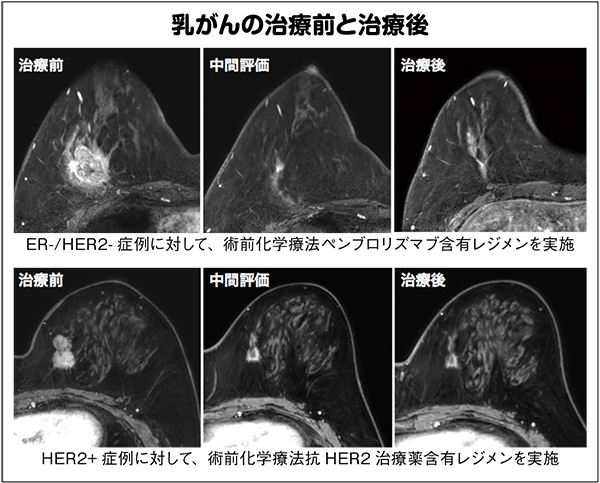
「トリプルネガティブ乳がんは、従来は予後が悪いものでしたが、免疫チェックポイント阻害剤の登場で予後が改善されました」(島講師)
ただし免疫チェックポイント阻害剤は、副腎不全や糖尿病、心筋症などの合併症のリスクがあるため、注意が必要だ。
以上、薬物治療について紹介したが、放射線治療や手術も行われる。
放射線治療は、乳房部分切除術後や、リンパ節転移が多くみられる場合にも放射線治療が推奨されている。
手術は①「乳房全切除術」と②「乳房部分切除術」が基本。それに加えて③「乳房再建」がある。
①「乳房全切除術」は、メスや電気メス、エネルギーデバイスを使い、乳腺組織と脂肪組織をしっかり切除する手術である。乳房の全部切除術により喪失感を伴うため、後述する③「乳房再建」を希望するケースが増えている。
②「乳房部分切除術」は、文字通り、乳房を部分的に切除してなるべく乳房を温存する手術だが、残った乳房に放射線を照射することが前提になるので治療方針全体を鑑みることが大切となる。
③「乳房再建」では、「ティッシュ・エキスパンダー」で組織を拡張した後に、シリコン製の「インプラント」を挿入する手術。インプラントではなく腹部や背中の自家組織(腹直筋皮弁や広背筋皮弁)を移植する「自家組織再建」も行われている。

【子宮頸がん】予後が劇的によくなる免疫チェックポイント阻害剤

子宮頸がんは、子宮体がん同様、ステージによって治療内容が異なる。
そのステージは「0期」から「Ⅳ期」まである。
「0期」は子宮の表皮(上皮)のごく一部に腫瘍が限局している場合(上皮がん)をいう。
「Ⅰ期」は「ⅠA1期」と「ⅠA2期」、「ⅠB1期」、「ⅠB2期」、「ⅠB3期」があり、「ⅠA1期」は腫瘍の上皮への浸潤の深さが3㍉以下の場合、「ⅠA2期」は3~5㍉の場合、「ⅠB1期」は腫瘍の大きさが2㌢以下、「ⅠB2期」は2~4㌢、「ⅠB3期」が4㌢以上と、分類される。
「Ⅱ期」は「ⅡA期」と「ⅡB期」があり、「ⅡA期」は腫瘍が子宮頸部を超えて膣の上部(基靭帯)まで広がっているものの、骨盤の壁(骨盤壁)や膣の下部に達していない状態、「ⅡB期」は子宮を支える組織(子宮傍組織)に広がっている状態をいう。
「Ⅲ期」は「ⅢA期」と「ⅢB期」があり、「ⅢA期」は腫瘍が膣の下部まで広がっているが、骨盤壁までには達していない状態、「ⅢB期」は骨盤壁まで達している場合をさす。
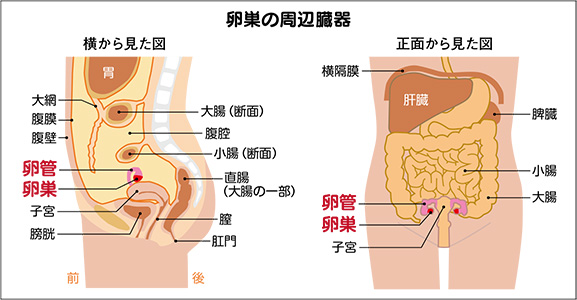
「Ⅳ期」は子宮の隣にある膀胱や直腸に転移する状態をいう(図1)。
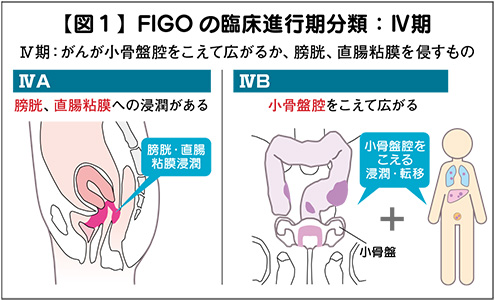
このように子宮頸がんのステージは複雑だが、それぞれのステージにおける治療を一覧にした(図2)。
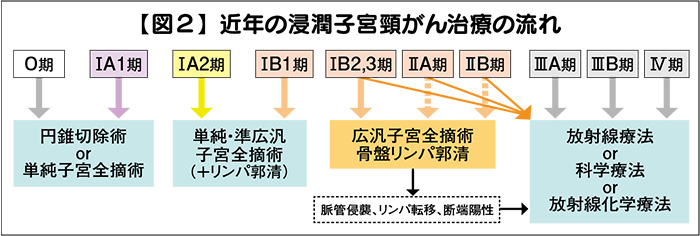
子宮頸がんの治療はⅠ「手術」とⅡ「放射線治療」、Ⅲ「化学療法」、Ⅳ「免疫療法」の4つ。
Ⅰ「手術」には①「円錐切除術」と②「子宮全摘術」がある。
①「円錐切除術」は、子宮の入り口(頸部)を削り取る手術。
②「子宮全摘術」は、文字通り、子宮を摘出する手術だが、手術の範囲に応じてア「単純」イ「準広汎」ウ「広汎」の3つに分けられる(図3)。
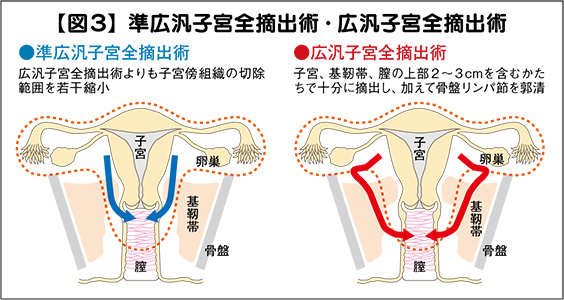
円錐切除術は、「0期」ないしは「ⅠA1期」の早期がんに行う。一方、子宮全摘術の方は、「Ⅰ期」から「Ⅱ期」にかけて行い、同時にリンパ節を摘出する「リンパ郭清」も行う。
「子宮全摘術では、かつては広い範囲の子宮を摘出する『広汎』が『Ⅰ期』の後半から『Ⅱ期』にかけて行われていたのですが、術後の合併症などを考慮して近年は子宮を摘出する範囲を縮小する『準広汎』へと変わりつつあり、リンパ節も全部取らないで一部のみを摘出する方法へと、縮小化・低侵襲化が最近の流れになっています」と、札幌医科大学産婦人科の齋藤豪教授。
前述の術後の合併症には、排尿障害やリンパ浮腫があるという。
子宮頸がんの治療には放射線治療も行われ、通常、放射線と抗がん剤を併せた「放射線化学療法」が行われている。
「放射線治療と手術では、予後に差がないと言われています。放射線治療にも膀胱炎や腸炎などの合併症のリスクがあり、すべて放射線治療が優れているとは言えませんが、縮小化・低侵襲化の流れから『Ⅱ期』については放射線治療を行うことが多くなってきました。『Ⅲ期』以上については、手術はできないので放射線化学療法になります」(齋藤教授)
化学療法では、かつては抗がん剤を使っていたが、分子標的薬療法が登場して、最近はそれが一般的に使われるようになった。主な分子標的薬はアバスチンで、従来の抗がん剤にアバスチンを加えた治療が行われている。
さらに免疫チェックポイント阻害剤による免疫療法も登場し、予後が劇的によくなっている。
「『Ⅲ期』や『Ⅳ期』の進行症例でも、ほぼ病変が消失して長期生存している方がいます」と齋藤教授。
【子宮体がん】抗がん剤&免疫チェックポイント阻害剤の併用が標準

産婦人科
渡利 英道教授
子宮体がんの治療は、ステージによって異なる。
がんが子宮体部に限局している状態がⅠ期で、 Ⅱ期はがんが子宮頸部(入り口)にまで広がっている状態をいう。
Ⅲ期は、がんが卵巣卵管にまで及んでいる状態(ⅢA期)や腟に転移している状態(ⅢB期)、リンパ節に転移している状態(ⅢC期)に分類される。
Ⅳ期のなかでⅣA期は、がんが子宮の周辺臓器に広がり腫瘍がひと固まりになっている状態、ⅣB期は、がんが肺や肝臓などの遠隔臓器に転移している状態をいう。
Ⅰ期からⅢ期までは手術で腫瘍を取り切れると判断できるケースが多いため、その場合は手術を行うが、Ⅳ期で遠隔転移がある(ⅣB期)と、手術で取り切れないこともあるので、その場合には抗がん剤などの薬物治療から始めることもある。
また腫瘍がひと固まりになっている場合(ⅣA期)には手術が適用にならないことがあり、薬物治療や放射線治療を行うこともある。
手術は、子宮と卵巣卵管の摘出が基本となる。子宮と卵管の摘出だけで完了すると考えられるのはⅠA期の一部だけで、それ以外はリンパ節を切除する「リンパ郭清」を行うことが多い。
「ある程度病気が進んでいくと、リンパ節に転移する可能性が高くなるのでリンパ節を採取して調べます。最近は内視鏡手術が普及しているのでⅠA期だと腹腔鏡を用いた子宮や卵巣卵管の摘出も多いです」と北海道大学産婦人科の渡利英道教授。ロボット支援による腹腔鏡手術も行われているという。
このように早期のがんについては、腹腔鏡手術を行うことが多いが、Ⅱ期以上になると開腹手術となる。
「最終的なステージは手術で決まります。画像検査である程度のステージを予想して、それに対して必要な手術を受けていただきます」(渡利教授)
一方、薬物治療では、抗がん剤と免疫チェックポイント阻害剤を併用するのが、いまのスタンダードな治療になっている。手術で切除しきれないと予想される場合や再発した場合などに適用となる。
抗がん剤はパクリタキセルとカルポプラチンを併用(TC療法)、それに加えて免疫チェックポイント阻害剤を使う。
抗がん剤と免疫チェックポイント阻害剤の併用療法は、3週間に1回行い、6コースが標準となる。
「6コースの抗がん剤治療が終わった後に、再発予防の観点から維持療法として免疫チェックポイント阻害剤だけを単独で使います」(渡利教授)
術後にがんが再発した場合には、レンバチニブのような分子標的薬と免疫チェックポイント阻害剤を併用する。
「免疫チェックポイント阻害剤で、明らかに生存率が上がっているというデータがあるので、再発の場合や切除不能の進行がんの場合には免疫チェックポイント阻害剤を提案しています」(渡利教授)
明るい話題として、乳がんの治療で使われている抗体薬物複合体(ADC)の「トラスツズマブデルクステカン」が年内にHER2高発現の子宮体がんの治療で使えるようになる。
HER2は子宮体がんの細胞増殖を促進させるが、この薬剤はHER2を目印にしてHER2にADCが結合することにより、がん細胞の中に抗がん剤を取り込みやすくする作用がある。
「子宮体がんでHER2が多く認められる人だと、ADCは8割程度効くというデータがあります。ただし間質性肺炎などの副作用のリスクもあるので、十分注意して使うことが大切です」と渡利教授。

【卵巣がん】再発までの期間を延ばす「維持療法」

産婦人科
片山 英人准教授
卵巣がんの治療は①手術と②薬物療法(抗がん剤治療、維持療法)がある。
手術は開腹手術で、子宮や卵巣卵管を切除し、小さな転移を見つけるために大網(脂肪の膜)を取って腫瘍の有無を調べたり、腹水の中の腫瘍の有無を調べ、早期がんの場合にはリンパ節を取って転移を調べる「リンパ郭清」を行う(基本術式)。
卵巣がんのステージは「Ⅰ期」と「Ⅱ期」が早期がん、「Ⅲ期」と「Ⅳ期」が進行がんと言われている。「Ⅲ期」「Ⅳ期」の進行がんの場合、2年以内に5割強が、5年以内に6~7割が再発する。5年生存率は「Ⅰ期」が90%、「Ⅱ期」が80%程度、「Ⅲ期」が50%強、「Ⅳ期」が40%強。
「肉眼では卵巣が割れておらず『Ⅰ期』に思えても顕微鏡で調べると腹水にがんが散って(腹膜播種)腹膜や腸管などに転移して『Ⅲ期』だったというケースもあります。手術や抗がん剤で腫瘍を限りなく『ゼロ』にして再発させないという考え方が基本です」と旭川医科大学産婦人科の片山英人准教授。
卵巣がんの場合、リンパ節転移よりも腹膜播種の方が治療に難渋するという。
抗がん剤治療では「パクリタキセル」や「カルボプラチン」を使い、進行がんには「べバシズマブ」を加えることがある。
前述したように、進行がんの場合、2年以内に5割強が再発するため、進行を遅らせて再発するまでの期間(無増悪期間)を延ばすのが維持療法だ。
「オラパリブ」、「ニラパリブ」、「ベバシズマブ」あるいは「オラパリブ」と「ベバシズマブ」の併用療法が行われる。遺伝子検査を行い、それによって維持療法を選択することになる。
「遺伝子検査で、遺伝子異常がみられた方は異常がみられない人と比べて、より維持療法の効果が期待でき、再発までの期間を延ばすことができます」(片山准教授)
卵巣がんは、初期症状がなく、気付いた時には進行している場合が多い。
「現段階では子宮がん検診はあっても、卵巣がん検診はありません。婦人科検診や子宮がん検診の際の超音波検査で『卵巣が腫れている』と診断され、受診を勧められた際には、ぜひ受診していただきたい」と片山准教授。

【不妊症】「タイミング法」&「人工授精」妊娠率が高い「ART」

岩見菜々子診療部長
不妊症の治療では、原因が判明した症例については、第一にその原因に対する治療を行う。
たとえば子宮内膜症による卵巣腫瘍がある場合には、子宮内膜症性嚢胞の治療を行う。子宮内に物理的な障害をきたすような子宮内膜ポリープや子宮筋腫などがある場合には、それらを切除する。ホルモンバランスの異常として甲状腺機能異常や、プロラクチンなどの排卵障害になるようなホルモン異常がある場合には、それらの治療を行う。
そのうえで、最初に始める不妊治療として①「タイミング法」(保険適用)がある。次に精子を子宮の中に注入する②「人工授精」(同)、そして体の外で受精卵をつくり(体外受精)、受精卵を体内に戻す(胚移植)といった③「高度生殖補助医療」(ART)(同)がある。
「当院ではこれらの治療について基本的にステップアップ方式を採用していますが、女性の年齢や不妊期間、不妊原因によって適用や優先順位が異なるので、必ずしもステップアップ方式を採るわけではありません」と神谷レディースクリニックの岩見菜々子医師。
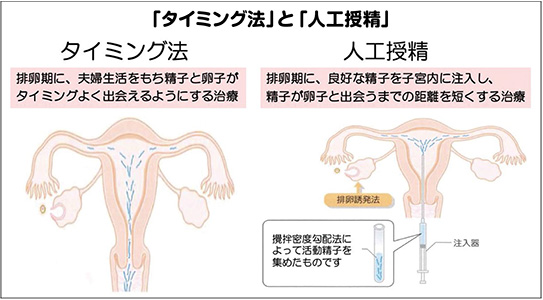
原因がなく、不妊期間が6ヵ月未満と短い場合には①「タイミング法」を行うことが多い。これは排卵日に合わせて性交渉してもらい、精子と卵子がタイミングよく出会えるようにする治療で最も自然に近い方法だ。
②「人工授精」は排卵日の直前・直後の時期に良好な精子を子宮内に注入し、精子が卵子と出会うまでの距離を短くする治療。子宮の入り口である頸管などに問題がある場合や精子の運動率が低い場合、精子の数が少ない場合(男性因子)などに適用になる。
①「タイミング法」や②「人工授精」については、排卵の数日前に受診して超音波検査や尿検査などで排卵日を予測。
「自然排卵が難しい場合には排卵発育目的に排卵誘発剤(内服薬)を用いて卵胞の発育を促します。これにより卵胞の発育を確認し、どちらの治療法も排卵に合わせた治療が可能となります」(岩見医師)
①「タイミング法」と②「人工授精」では男性因子がない場合には妊娠率にそれ程差はなく、通常2~3%と言われている。
③「高度生殖補助医療」(ART)は、受精卵を体外で培養し、子宮の中に着床するところまで成育させた後に子宮の中に移植する治療だ。卵子を体の外に取り出す「採卵」を行うが、1回の採卵で複数の卵子を回収する方が受精卵を得られるチャンスが広がる。そのため月経周期2~3日目から10~12日間の連日、患者に排卵誘発剤(注射薬)の自己注射をしてもらい、卵胞の発育をモニタリングしながら採卵を行う。採卵した卵子は採卵当日に精子と受精させる。その際、卵子に精子をふりかけ自然な力で受精させる方法が「体外受精」だ。
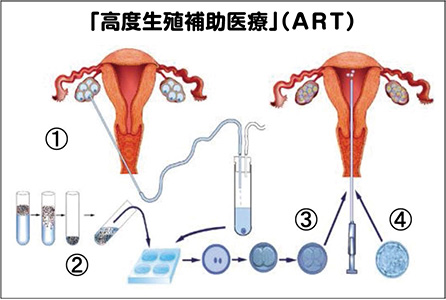
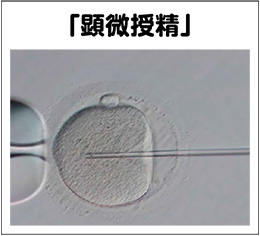
だが、受精障害や精子の数が少ない、運動率が低い場合には受精が難しくなるため、卵子に精子を直接針で注入する方法が用いられる。これが「顕微授精」である。
「体外受精」でも「顕微授精」でも採卵の翌日に受精の有無を確認し、受精が確認された受精卵は培養器で受精卵(胚)を体外でモニタリングしながら培養し、良好な受精卵ができたらその受精卵を一旦凍結するか、同一周期で子宮の中に戻す(胚移植)。
日本では90%以上の医療機関で胚移植を排卵周期とは別の周期に行う「凍結融解胚移植」を行っている。受精卵を液体窒素で一度凍結保存し、患者の体の状態が通常の状態に戻ってから改めて胚移植する方法だ。
この方法だと卵巣過剰刺激症候群のリスクを抑制することができ、ホルモンバランスとしても妊娠率が高くなり、最新のデータでは1回の胚移植で35歳未満の方で65%以上、35~38歳で55%、38~40歳で46%、41~43歳で42%、44歳で12%以上が妊娠している。
「不妊治療で約8・5人に1人が高度生殖補助医療(ART)で出産しており、一般的な治療になっています。35歳以上で一般不妊治療や人工授精を4~6回行っても妊娠が成立しない場合には、できるだけ早くARTを検討していただくことをお勧めしています」と岩見医師。
ただし、この治療には卵巣過剰刺激症候群という合併症のリスクがあり、その予防が大切だ。卵巣を排卵誘発して刺激することで卵巣が肥大したり、腹水がたまったり、重症化すると血栓ができる。その予防の治療を併せて行うことやトリガー(採卵の直前に卵子を成熟させるための刺激)を工夫することで、合併症を90%以上予防することができる。
一方、不妊の原因が男性にある場合(男性不妊)には、前述の顕微授精が必要で、顕微授精を行えば女性の年齢層に応じた妊娠率が期待できる。

